Kwaliteit van Leven bij primair hyperaldosteronisme (PHA) na behandeling met medicijnen of na een operatie – verdiepingsartikel
Aanleiding
Op het forum van de Bijniervereniging NVACP zijn een aantal patiënten met elkaar “in gesprek” over primair hyperaldosteronisme (PHA) (najaar 2022 en voorjaar 2023). Zij wisselen ervaringen uit over de periode na de operatie waarbij een bijnier is verwijderd of na de start met medicijngebruik met Spironolacton of Eplerenone. Zij missen een deel van de informatie die in de afgelopen jaren is gepubliceerd in vaktijdschriften over endocrinologie.
In 2022 is bijvoorbeeld een artikel verschenen waarin een weergave wordt gegeven van interviews met 25 patiënten, die hun ervaringen delen met de onderzoekers over de tijd voor de diagnose, de diagnose zelf, de tijd na de diagnose en de behandeling. Daarnaast waren er twee artikelen1, 2 over de kwaliteit van leven (QoL) na de start van de behandeling na 6 en 12 maanden.
Het onderzoek naar de QoL is gedaan bij 200 patiënten in Nederland en Polen met gestandaardiseerde vragenlijsten2.
Inleiding
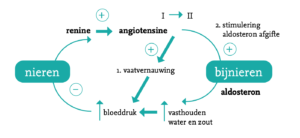
Bij primair hyperaldosteronisme wordt er in de bijnieren te veel van het hormoon aldosteron gemaakt. Meestal is er sprake van een aldosteron producerend adenoom (APA) (enkelzijdig) of bilaterale (tweezijdige) bijnier hyperplasie (BAH) = (vergroting van de bijnieren). Het hormoon aldosteron heeft invloed op de water- en zouthuishouding in het lichaam. Bij een te hoog gehalte aan aldosteron zal er een verhoogde bloeddruk en vaak een laag gehalte aan kalium in het lichaam ontstaan. Dit geeft een bijkomend risico op hart- en vaatziekten, zoals TIA (herseninfarct van voorbijgaande aard), CVA (herseninfarct of hersenbloeding), myocardinfarct (hartinfarct) en verminderde nierfunctie.
Hoewel PHA veel voorkomt, krijgen de meeste patiënten geen juiste diagnose. De schatting is dat bij 5-15% van de patiënten met een verhoogde bloeddruk PHA hiervan de oorzaak is. Er is een grote onderdiagnose, slechts bij minder dan 5% wordt een correcte oorzaak aangewezen. De verhoogde bloeddruk wordt vaak bij toeval gevonden, vaak hebben patiënten nauwelijks klachten van een verhoogde bloeddruk. Daarom is het belangrijk om minstens één keer per jaar de bloeddruk te (laten) meten.
De verhoogde bloeddruk wordt veelal behandeld met medicijnen die de bloeddruk verlagen. De gebruikelijke medicatie slaat bij PHA niet (voldoende) aan. Er zijn 2 medicijnen (mineralocorticoïdreceptorantagonisten) die goed werken nl. Spironolacton en Eplerenone. Het is sterk aan te bevelen dat wanneer de gebruikelijke medicatie om de bloeddruk te verlagen niet goed aanslaat, er verder onderzoek wordt gedaan naar de aldosteron/renine ratio (ARR) en naar kalium. Helaas gebeurt dit te weinig.
In diverse artikelen wordt aangegeven dat er een te sterke onderdiagnose is3 Het is niet juist om er als arts dan van uit te gaan dat als de bloeddruk niet (voldoende) daalt dat de patiënten dan hun medicatie niet goed zouden innemen.
Diagnose en de tijd voor de diagnose
Over het algemeen duurt het lang voor de diagnose primair hyperaldosteronisme (PHA) wordt gesteld. Patiënten hebben vaak langdurige klachten die voor een deel zijn terug te voeren op de hoge bloeddruk maar zeker ook op het verhoogde gehalte aan aldosteron en/of op het lage kalium. Bij een verlaagd kalium kunnen spierproblemen ontstaan omdat het kalium wordt onttrokken aan het spierweefsel om daarmee kalium in het bloed op peil te houden (het hart is ook een spier).
Problemen voorafgaand aan de diagnose zijn naast de spierproblemen ernstige vermoeidheid, depressieve gevoelens, angst en gedragsproblemen. Deze combinatie maakt dat je niet meer helder kan denken, het concentreren is moeilijk en mensen raken gauw geïrriteerd (‘kort lontje’). Daarnaast zijn vermoeidheid en (soms) hartkloppingen aanwezig. Je kunt dus rustig spreken van een sterke vermindering van kwaliteit van leven. Overigens iets waar patiënten met andere bijnieraandoeningen ook over klagen.
Minstens zo hinderlijk was het lange uitblijven van de diagnose en daardoor het idee dat je een aansteller bent. Daar komt later het gebrek aan kennis nog bij. Gebrek aan kennis (voorlichting) is er niet alleen bij patiënten, maar zeker ook bij huisartsen, internisten en verpleegkundigen. Daarom probeert BijnierNET nog steeds nieuwe informatie aan te dragen voor iedereen die het nodig heeft.
Het is een opluchting als je eindelijk de juiste diagnose krijgt, informatie en uitleg kunt vinden en je kunt gaan werken aan herstel. Of in ieder geval kunt gaan werken aan verbetering van de kwaliteit van leven. Dit kost veel tijd en lukt vaak niet helemaal.
Diagnosestelling
De manier en de volgorde van de testen worden beschreven in de informatiebrochure PHA op de website van BijnierNET.
De volgorde van testen is ARR-test (Aldosteron/Renine Ratio) om de ziekte aan te tonen, zoutbelastingtest om de ziekte te bevestigen. Zijn beide testen afwijkend en dus wijzend op PHA, dan wordt gekeken of de overmaat aan aldosteron uit één bijnier komt of uit allebei. Dit onderzoek heet AVS. Dit is de Engelse afkorting voor Adrenal Veinous Sampling, in het Nederlands: bloedmonster uit beide bijnieraders. De bloedmonsters worden genomen om te zien in welke bijnier het meeste aldosteron wordt geproduceerd, of dat beide bijnieren (ongeveer) evenveel aldosteron overproduceren. Als het verschil in productie groot genoeg is, zal de meest producerende bijnier worden verwijderd. Komt de overproductie uit beide bijnieren, dan volgt een (levenslange) behandeling met medicijnen. De AVS kan het beste worden uitgevoerd in een expertcentrum waar veel ervaring is met het uitvoeren van de test.
Een CT-scan of MRI geeft inzicht in de ligging en grootte van het adenoom. Is het adenoom groter dan 5 cm dan is er een verhoogd risico op kwaadaardigheid. Het adenoom/de bijnier zal dan sowieso preventief worden verwijderd, ongeacht vanuit welke bijnier er teveel aldosteron wordt geproduceerd.
Bij deze testen kunnen bepaalde medicijnen niet gebruikt worden omdat die het resultaat van de test vertekenen. Er zijn dan wel andere medicijnen die je wél kunt gebruiken. Ook moet het kalium op peil zijn om tot een goede test uit te kunnen voeren.
Behandeling
Bij enkelzijdig PHA wordt bijna altijd de aangetaste bijnier verwijderd. Soms lukt het om alleen het adenoom te verwijderen. De operatie wordt bij voorkeur gedaan in een ziekenhuis met expertise in deze operaties. Het gebeurt meestal met een kijkoperatie via de rug. Dit is afhankelijk van de ervaring van de chirurg, maar het voordeel is dat de bijnier makkelijker bereikbaar is via de rug en dus de kans op mogelijke complicaties kleiner is.
Bij dubbelzijdig PHA wordt er zelden geopereerd en bijna altijd behandeld met mineralocorticoïdreceptorantagonist in de vorm van Spironolacton of Eplerenone, soms aangevuld met amiloride. Spironolacton kent behoorlijk veel bijwerkingen. Vooral ontwikkeling van vrouwelijke eigenschappen bij een man (anti-androgene bijwerkingen van MRA’s) komt vaak voor. Dit zijn gynaecomastie (borstontwikkeling), mastopathie (gespannen, pijnlijke borsten), menstruatiestoornissen, erectiestoornissen en verminderd libido (seksuele opgewondenheid, zin in seks).
De kwaliteit van leven verbetert op de lange duur heel behoorlijk, zowel na een operatie als ook met medicijnbehandeling. Bij de medicijnbehandeling neemt de kwaliteit veel langzamer toe en dat verschil is goed merkbaar na een half jaar. Na een jaar is de kwaliteit bijna gelijk volgens de gemelde onderzoeksresultaten.
Verbetering van de kwaliteit van leven (QoL)
Het meten van de QoL gebeurt over het algemeen met gekwalificeerde vragenlijsten, waarna er met behulp van statistiek gemiddelde conclusies worden getrokken. Dit is ook gebeurd bij een groot onderzoek in Nijmegen (2017) bij ongeveer 200 patiënten2. De meetmomenten zijn na 6 en 12 maanden.
Na 6 maanden is de QoL na de operatie beter dan bij medicijnbehandeling.
Patiëntenervaring ná de operatie
Wat veelal niet wordt vermeld in (wetenschappelijke) artikelen is hoe moeilijk patiënten de tijd na de operatie ervaren. De ervaringen van patiënten beschreven op het forum van de Bijniervereniging NVACP zijn zwaar4. De klachten zijn vooral ernstige moeheid en die belemmert vrijwel iedereen in de eerste maanden om zijn of haar leven weer op te bouwen. De verbetering komt wel, maar de stapjes zijn klein en vragen veel geduld van de patiënt en zijn omgeving. Dat laatste wordt vooral als een probleem ervaren. Het is vrijwel niet uit te leggen dat je nog steeds heel moe bent terwijl de operatie toch al weer weken is geleden. Die zelfde ervaring hebben patiënten die medicijnen met MR-antagonisten (Spironolacton en Eplerenone) worden behandeld ook. Wel wordt ervaren dat het denken en het concentratievermogen langzaam beter wordt, je wordt helderder in je hoofd. Uit eerder gedeelde ervaring blijkt dat er patiënten zijn die ook na een jaar nog problemen ervaren. Het lijkt erop dat dit vooral bij dubbelzijdig PHA is, waar de patiënten met medicijnen worden behandeld. Let wel: dit zijn de ervaringen van enkele patiënten bij wie het herstel niet zo vlot verloopt als gehoopt. Wellicht schrijven de patiënten bij wie het herstel sneller en zonder grote problemen verloopt, niet op het forum. Het maakt wél duidelijk dat er dus grote verschillen zijn tussen patiënten in hoe het herstel verloopt.
Een vraag is of een deel van de blijvende problemen worden veroorzaakt door de jarenlange tijd met hoog aldosteron en een hoge bloeddruk en een laag kalium? Helaas is daar weinig over te vinden in de literatuur.
Sinds kort is er ook een test beschikbaar waarmee een DNA-profiel kan worden vastgesteld om te zien hoe snel medicijnen worden afgebroken. Door vooraf te bepalen of iemand het medicijn veilig kan gebruiken voorkom je problemen. Met deze test maak je met een klein stukje DNA een farmacogenetisch paspoort5, 6.
Conclusie
PHA is een ernstige aandoening die laat of niet wordt gediagnosticeerd. Dit heeft consequenties voor de kwaliteit van leven (QoL). Die is vaak sterk verminderd.
Patiënten voelen zich vaak niet serieus genomen vóór de diagnose en missen informatie en kennis tijdens en na de diagnose. Vooral de eerste maanden na de operatie of na de start met medicatie (waarvan de dosering vaak nog aangepast/ingeregeld moet worden) kunnen heel zwaar zijn. Deze periode vraagt veel van patiënten en daar mag wel meer begrip voor zijn. Begrip van de omgeving maar ook van de zorgverleners4 .
Het langdurig verhoogde aldosteron en daardoor de hoge bloeddruk en laag kalium kan leiden tot verschillende bijkomende aandoeningen (comorbiditeiten)1. Een aantal worden altijd wel genoemd, maar over andere bijwerkingen wordt weinig aangegeven. De klachten zijn dan te onduidelijk of roepen geen herkenning op. Toch hebben patiënten er vaak veel last van en zij vinden geen erkenning van hun klachten.
Er zou meer onderzoek moeten worden gedaan naar het “grijze gebied” en de “vaag” benoemde klachten.
Een nadeel is dat de ervaringen afkomstig zijn van een beperkte groep patiënten waardoor er weinig gezegd kan worden over het vóórkomen (prevalentie) van de klachten. De publicaties1 over de diverse comorbiditeiten zijn ook afkomstig van kleine onderzoeksgroepen.
Dat is op zich niet erg. Het benadrukt alleen dat er een grote spreiding is in de kwaliteit van leven vóór en na de diagnose.
Referenties:
- Anxiety, Depression, and Impaired Quality of Life in Primary Aldosteronism: Why We Shouldn’t Ignore It! Martin Reincke JCEM 2018 103(1):1-4.
- Quality of Life in Primary Aldosteronism: A Comparative Effectiveness Study of Adrenalectomy and Medical Treatment.
Marieke Velema, en anderen
The Journal of Clinical Endocrinology & Metabolism 2018 103(1):16-24. - Illness perspectives in patients with primary aldosteronism
Door Oskar Ragnarsson en anderen. PLoS ONE 17(11): e0277902 - Patiëntenforum op de website van de Bijniervereniging NVACP
- Artikel DNA testen voor bijwerkingen A12-gene farmacogenetisch paspoort
- Veel gestelde vragen farmacogenetisch paspoort
Deze webpagina is onder auspicien van het bestuur van BijnierNET geschreven door Margot Ekhart en Alida Noordzij vanuit hun rol als ervaringskundigen in april 2023 en gepubliceerd in juni 2023.
